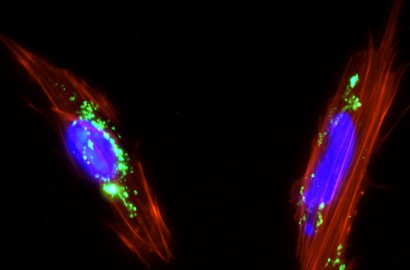
Su sistema para identificar patógenos genéticamente puede acelerar los diagnósticos desde los dos días hasta solo cuatro horas.
La genómica está llamada a ser la gran revolución de la medicina en el siglo XXI. Además de su capacidad para favorecer los tratamientos personalizados, los análisis genéticos también pueden transformar el campo de los diagnósticos, cuyas técnicas actuales tienden a ser costosas, lentas y poco precisas. Pero esto puede estar a punto de cambiar gracias al sistema creado por el joven Daniel Ortiz, capaz de analizar patógenos a partir de una muestra de ADN y acelerar la obtención de resultados desde los dos días que se tardan ahora hasta solo cuatro horas. Gracias a esta innovación Ortiz se ha convertido en uno de los ganadores de Innovadores menores de 35 Colombia 2016 de MIT Technology Review en Español.
El proceso usa un método existente de análisis de ADN a partir de una muestra de sangre de un paciente con una patología. Primero se cultiva el patógeno desconocido y se aísla su gen 16s. Este gen está presente en todas las bacterias y contiene información que permite identificarlas. Una vez detectado, se amplía, se calienta y se mide su fluorescencia, ya que las moléculas de ADN en su estado natural generan una fluorescencia brillante. Cuando se calientan entre 45 °C y 95 °C, las hebras se van separando, y a medida que lo hacen van perdiendo fluorescencia. Esta pérdida de brillo progresiva genera una curva, que es distinta y característica para cada bacteria. Y mediante algoritmos propios, Ortiz las analiza para descubrir de qué bacteria se trata.
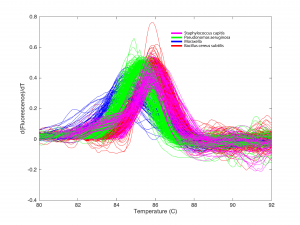
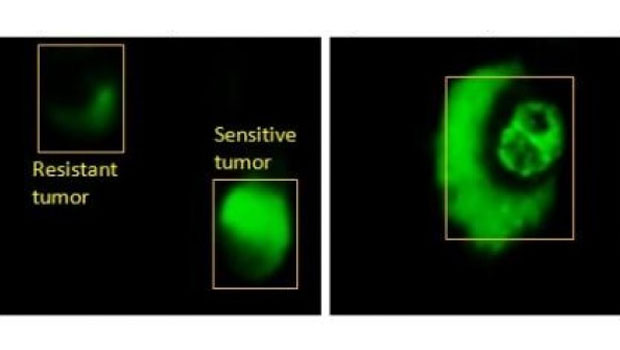
Típicas curvas de pérdida de fluorescencia adquiridas de un chip en el cual se incluyó el ADN de 5 tipos de bacteria conocidos. Cada color representa a un patógeno distinto. Crédito: Hannah Mack.
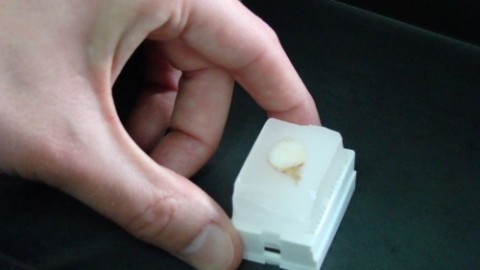
El joven emplea un microchip de un centímetro cuadrado con 20.000 contenedores para depositar 20.000 moléculas. En ellos se coloca la muestra de sangre y se obtiene la curva de cada una de las moléculas. El resultado es lo que el joven denomina como huellas dactilares moleculares. Gracias a ellas es posible «diferenciar varias bacterias y detectar si una persona tiene en su organismo más de un patógeno para recomendar el antibiótico más adecuado», explica. Para calentar la muestra emplea un cubo cuyas aristas miden 10 centímetros, y también necesita un microscopio de medio metro para medir la fluorescencia. El objetivo actual de Ortiz es reducir el microscopio para hacerlo más portable.
El sistema ha sido creado en el departamento de Bioingeniería de la Universidad de California en San Diego (EEUU) donde Ortiz realiza su doctorado con la doctora Stephanie Fraley. Ya han realizado pruebas con muestras de patógenos y ahora solo les falta empezar a trabajar con muestras humanas reales. Ortiz es optimista y cree que en un futuro próximo su idea puede convertirse en parte de la práctica clínica al sustituir a los «cultivos tradicionales, que requieren casi dos días de espera y la presencia de un microbiólogo».
El avance de este joven puede tener «un alto impacto», según la inversora ángel en Tecnología en Calligram (España) y miembro del jurado de Innovadores menores de 35 Colombia 2016, Paloma Cabello. En su opinión, Ortiz «parece haber tomado estudios anteriores como base para avanzar añadiendo capacidades avanzadas de computación y miniaturización».
Fuente:
Technology Review