Un equipo de investigadores de la Universitat Politècnica de València (UPV), el Instituto de Investigaciones Biomédicas «Alberto Sols» (CSIC-UAM), la Universitat de València y el CIBER de Bioingeniería, Biomateriales y Nanomedicina (CIBER-BBN, dependiente del Instituto de Salud Carlos III), ha desarrollado, a escala de laboratorio, nuevos nanodispositivos que permiten la liberación controlada de fármacos -en concreto, doxorrubicina- para terapias contra el cáncer de mama.
Hasta el momento, los trabajos, que han sido publicados en el Chemistry-A European Journal, se han centrado en ensayos celulares. Según los investigadores, los resultados han sido «positivos», y «podrían abrir nuevas vías para mejorar la eficacia de algunos fármacos aplicados en el tratamiento del cáncer de mama».
Cada nanodispositivo controla cuándo y dónde libera el fármaco transportado
La principal novedad de los nanodispositivos diseñados es que la molécula que los recubre no sólo controla cuándo se libera el fármaco transportado, sino también dónde, gracias a su direccionamiento hacia células que expresan TLR3, una proteína del sistema inmunitario innato que se encuentra sobreexpresada en algunas líneas celulares de cáncer de mama. A través de esta proteína, se lanza una señal que acaba con la célula tumoral.
Amelia Ultimo, investigadora del Instituto Interuniversitario de Investigación de Reconocimiento Molecular y Desarrollo Tecnológico (IDM) en la UPV, explica que, «además, la propia puerta molecular posee un efecto citotóxico en células de cáncer de mama. De este modo, la molécula que utilizamos como puerta es capaz de generar tres acciones clave: ayuda a dirigir el fármaco hacia el receptor TLR3, inhibe la liberación del mismo hasta que no llega al punto deseado y, a través de la interacción con el receptor, activa un proceso de muerte celular».
¿Cómo actúa?
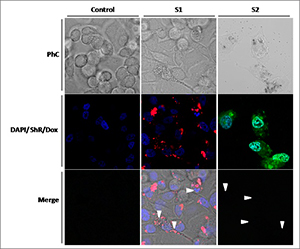
La interacción entre la puerta molecular y el receptor resulta fundamental para la posterior liberación del fármaco dentro de las células tumorales. Gracias a este reconocimiento, los nanodispositivos pueden ser internalizados en éstas mediante un proceso de endocitosis.
Una vez en el interior celular, la puerta molecular es degradada por las enzimas lisosomales, lo que permite la liberación de la doxorrubicina, que se intercala entre las hebras de DNA y es capaz de bloquear la replicación de las células afectadas. Este efecto citotóxico se suma sinérgicamente al de la puerta molecular.
Según destaca Ramón Martínez Máñez, director del IDM y máximo responsable científico de CIBER-BBN, las pruebas realizadas a nivel celular han constatado que los nanodispositivos desarrollados aumentan la eficacia terapéutica respecto al uso de RNA de doble cadena libre, debido a un efecto de aumento de la concentración al encontrarse nanoformulado. Además, la liberación en el interior celular de la doxorrubicina contribuye a disminuir la viabilidad de las células cancerígenas.
El cáncer de mama, el más letal entre las mujeres a nivel mundial
El cáncer de mama es el tumor más letal entre las mujeres a nivel mundial. No en vano, representa el 25% de todos los casos de cáncer y el 15% de las muertes por esta patología.
Su incidencia es especialmente alta en los países desarrollados, y afecta fundamentalmente a mujeres mayores de 65 años. Por ello, la investigación destinada a la identificación de nuevas terapias o a la mejora de las ya existentes es un campo, en la actualidad, de intensa actividad.